Atom dikenali sebagai komponen yang paling asas yang membentuk semua bahan-bahan dalam alam semesta.
Struktur asas atom adalah sama dengan sistem suria kita yang terdiri daripada matahari yang dikelilingi oleh planet-planet lain yang bergerak mengelilingi matahari mengikut laluan orbitnya.
Struktur atom terdiri daripada nukleus dan elektron yang bergerak di seluruh ia mengikut orbitnya.
Bahan yang paling asas atau bahan yang diketahui ialah hidrogen yang mempunyai pembinaan yang paling asas atom.
Rajah 1: pembinaan atom
Atom terdiri daripada nukleus yang mengandungi neutron dan proton, neutron adalah caj neutral manakala proton yang bercas positif. Elektron bercas negatif dan zarah elektron sentiasa mengorbit nukleus.
Nombor atom dan jisim atom relatif
Nombor atom mewakili bilangan proton dalam nukleus yang juga menunjukkan bilangan jumlah elektron di orbit.
Sejak atom terlalu kecil untuk diukur, jisim atom relatif yang digunakan untuk menunjukkan jisim atom. Atom Hidrogen digunakan sebagai rujukan, sekali gus memberikan jisim relatif 1. Jumlah jisim relatif akan menunjukkan atom besar-besaran berbanding dengan jisim hidrogen.
Contoh 1: -
Satu atom cooper mempunyai nombor atom 29 dan jisim relatif 63.
a) hitungkan bilangan proton dalam nukleus
b) mengira bilangan elektron dalam nukleus
c) calculatenumberofneutroninthenucleus
Penyelesaian; -
a) kerana nombor atom 29, sekali gus 29 proton dalam nukleus
b) 29 proton dalam nukleus yang bererti bahawa 29 elektron juga dalam orbit
c) numberofneutron = relativemass-atomicnumber = 63-29 = 34
Susunan elektron dalam orbit.
Elektron disusun dalam orbit yang dinyatakan ketika beredar mengelilingi nukleus.
Rajah 2: orbit elektron
Kami menetapkan orbit dengan bilangan n. Orbit paling dalam n = 1 akan terdiri maksimum 2 elektron, manakala orbit yang lain akan mempunyai maksimum 8 elektron untuk mencapai kestabilan.
Oleh itu, merujuk kepada contoh sebelumnya cooper atom,
Contoh 2: - menulis konfigurasi elektron bagi atom cooper
Penyelesaian: -
Sejak beberapa proton adalah 29, bermakna 29 elektron terdiri atas orbitnya. Konfigurasi elektron akan: -
n = 1 - 2 elektron
n = 2:-8electron
n = 3:-8electron
n = 4: - 8electron
n = 5; - 3 elektron
Oleh itu, jumlah elektron; - 29
Nombor Avogadro
Seorang saintis bernama Avogadro, telah ditemui dari eksperimen di atas karbon-12. Sejak hidrogen adalah sukar untuk digunakan dalam eksperimen, karbon-12 digunakan sebagai rujukan.
Dari eksperimen beliau, Avogadro ditakrifkan sebagai 1 mol
dan juga mendapati bahawa 1 gram-bahan tahi lalat akan mempunyai 6.023 x1023 atom.
Dari penemuan ini, kita boleh mendapatkan pengetahuan tambahan dari bahan kami
Contoh 3: - Memandangkan massa atom cooper adalah 63,54 g / mol
Kira: -
a) jisim 1 atom cooper b) bilangan atom dalam 1 gram cooper
penyelesaian: -
a) kerana jisim atom cooper adalah 63,54 g / mol, dan dari Avogadro, 1 mol = 6,023 x 1023 atom
sejak 1 mol = 6.023 x 1023 atom
demikian: - bilangan atom dalam 1 gram cooper = bilangan mol x Avogadro berterusan
= 0.01574 x 6.023 x 1023 = 9.47 x 1021 atom.
Hampir semua elemen asas di bumi ditemui dan dicatatkan di dalam carta dipanggil carta berkala.
Carta ini telah dibangunkan oleh ahli kimia Rusia Dmitri Mendeleev. Semua bahan-bahan asas yang disusun mengikut nombor atom dan saiz orbitlal elektron.
Hasilnya: -
Rajah 3: - carta berkala
Kita boleh mendapatkan maklumat daripada nombor atom, jisim relatif, sekumpulan bahan-bahan dan konfigurasi atom bahan asas.
ikatan atom
Ia amat jarang berlaku bahawa bahan tulen digunakan untuk tujuan kejuruteraan. Kebanyakan bahan-bahan yang digunakan adalah gabungan atau reaksi daripada beberapa bahan asas untuk membentuk bahan-bahan baru.
Atom bon antara satu sama lain oleh ikatan 3 jenis utama
bon logam
Rajah 4: ikatan logam dalam logam
Nucleus logam disusun pada struktur kristal manakala elektron akan bergerak secara bebas membentuk awan elektron pada permukaan logam. Ini akan bon atom dan membentuk satu ikatan yang kukuh di antara atom.
ikatan ionik
Borang ikatan apabila bahan logam tinggi (caj positif) dan bahan bukan logam tinggi (caj negatif) bertindak balas untuk membentuk bahan baru.
Rajah 5: Tindak balas antara natrium (logam) dan klorin (bukan logam)
Memandangkan natrium atom, yang terdiri daripada 1 elektron pada orbit paling luarnya. Sejak 8 elektron diperlukan untuk menstabilkan orbit, ia adalah mudah bagi atom natrium kehilangan 1 elektron untuk menjadikannya stabil dan bukannya menambah 7 elektron, sekali gus kehilangan 1 elektron akan membuat natrium atom positif caj, kita menetapkan atom natrium sebagai: -
Na + (natrium ion)
Klorin, kami mendapati bahawa ia mempunyai 7 elektron dalam orbit paling luar, dan dengan itu, untuk membuat stabil, ia hanya memerlukan 1 atom lagi untuk membuat ia 8. Oleh itu, sejak natrium perlu mengeluarkan 1 elektron dan klorin memerlukan 1 elektron, natrium akan menderma elektron untuk natrium, natrium itu akan dikenakan negatif sejak add 1 yang elektron, kita menetapkan atom klorin sebagai: -
Cl-(klorin ion)
Kedua-dua positif dan negatif ion caj akan menarik antara satu sama lain dengan teliti dan membentuk satu ikatan yang memanggil ikatan ion.
Kita boleh menulis persamaan tindak balas sebagai
Na + Cl → Na + + Cl-→ NaCl
Rajah 6: Ilustrasi pembentukan ikatan ionik
ikatan kovalen
Walaupun bentuk ikatan ionik dengan tarikan bertanggungjawab, ikatan kovalen adalah bentuk daripada perkongsian elektron orbit.
Ikatan kovalen terbentuk apabila 2 atau lebih bahan bukan logam bertindak balas.
Rajah 6: karbon atom bertindak balas dengan atom hidrogen membentuk ikatan kovalen
Dalam hal tindak balas karbon dengan hidrogen, kita akan melihat karbon yang mempunyai 4 elektron di orbit paling luarnya, bermakna ia memerlukan 4 lebih elektron untuk menjadikannya stabil.
Walaupun hidrogen hanya mempunyai 1 elektron pada orbit paling luar, kerana ini adalah orbit n = 1, ia hanya memerlukan 1 elektron lagi untuk membuat ia stabil.
Oleh itu, semasa tindak balas, hidrogen akan berkongsi elektron dengan karbon, dalam kes ini 4 atom hidrogen yang diperlukan itu menjadikan semua 4 atom hidrogen mempunyai 2 elektron dan atom karbon mempunyai 8 elektron.
Struktur kristal dan struktur bukan kristal
Atom di dalam bahan-bahan yang mempunyai perkiraan sendiri khusus yang kristal dan bukan kristal.
Struktur kristal: - atom disusun konsisten dalam konfigurasi tertentu.
Bukan kristal: - atom disusun secara rawak
struktur kristal
Satu struktur kristal terdiri daripada motif, satu set atom disusun dalam cara yang tertentu, dan kekisi. Motif yang terletak di atas titik kekisi, yang merupakan pelbagai mata mengulangi berkala dalam tiga dimensi.
Ini dipanggil sel unit.
Satu struktur kristal dan simetri memainkan peranan dalam menentukan banyak ciri-ciri, seperti perpecahan, struktur band elektronik, dan harta optik.
Terdapat 3 jenis kristal yang paling biasa: -
Badan Berpusatkan Cube (BCC)
Rajah 7: Badan berpusatkan kristal kiub
Seperti yang kita dapat bayangkan, ia adalah seperti mempunyai 1 atom di pusat yang dikelilingi oleh 8 atom mana kekisi adalah dalam bentuk kiub.
Bayangkan kita boleh mengambil 1 unit sel,
Rajah 8: BCC unit sel
Satu sel unit BCC terdiri: -
Oleh itu, jumlah atom dalam struktur BCC ialah 2
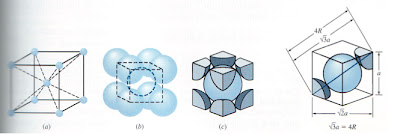
Wajah Cube Berpusatkan (FCC)
Struktur kristal yang mengandungi satu atom di tengah-tengah enam sisi kiub dan satu atom di setiap penjuru kiub. Logam dengan struktur kristal padu berpusat muka cenderung untuk menjadi mulur.
Rajah 9: Wajah berpusatkan kiub struktur sel unit
Bayangkan kita boleh mengambil 1 unit FCC,
Rajah 10: Wajah kiub berpusat unit sel
Sel unit FCC terdiri: -
8 unit atom dalam sudut kekisi kiub
6 unit atom dalam pesawat kekisi
Oleh itu, jumlah atom dalam struktur FCC adalah 4
Berbanding dengan BCC, FCC mempunyai lebih atom setiap sel unit menjadikan ia lebih padat dan tebal.
Struktur ini dipanggil struktur penuh ditutup.
Struktur Makan tertutup heksagon (HCP)
Rajah 11: - Struktur HCP
Atom disusun dalam cara yang unik banyak. Ia terdiri daripada kapal terbang 2 heksagon sandwiching satah segi tiga di bahagian tengah.
Jika kita boleh mengambil sel unit HCP
Satu heksagon pesawat akan mempunyai: -
- 6 unit atom di sudut dan atom di tengah-tengah heksagon
jumlah atom dalam heksagon pesawat = 1 atom. Oleh itu untuk 2 pesawat heksagon, jumlah atom = 3 atom
- 3 atom di tengah-tengah kekisi itu, jumlah atom dalam struktur HCP adalah = 3 +3 = 6 atom
Analisis menggunakan struktur unit
Kita boleh mendapatkan beberapa maklumat dari satu sel unit.
Badan kiub berpusat
Rajah 12: konfigurasi kekisi BCC
Pengukuran kekisi, yang boleh dilakukan dengan menggunakan teknologi canggih hari ini seperti x-ray teknik pembelauan.
Dengan mengetahui panjang kekisi, saiz atom tunggal boleh dianggarkan dengan tepat.
Merujuk kepada angka 12, dengan menggunakan teorem Pythagoras, saiz kekisi yang berkaitan dengan jejari atom diberikan oleh

Jika saiz kekisi dan R adalah jejari atom.
Wajah Cube Berpusatkan
Rajah 13: FCC kekisi konfigurasi
Menggunakan teknik yang sama, untuk FCC, saiz kekisi yang berkaitan dengan jejari atom diberikan oleh: -

Faktor pembungkusan Atom (APF) dan ketumpatan
APF (faktor pembungkusan atom) sebagai petunjuk bagaimana dibungkus struktur itu,

Contoh: -
Satu bahan berstruktur BCC mempunyai pemalar kekisi, a = 0,2665 nm. Kira: -
a) faktor
b) ketumpatan atom pembungkusan bahan-bahan jika berat bahan-bahan 12 g mol-1
Penyelesaian: -
a)
Untuk bcc,
Oleh itu: -
0,1154 nm unit isi padu sel = a3 =
= 0,0189 nm3 sejak 2 atom dalam sel unit 1 bcc, sekali gus jumlah atom =
= 0,0129 nm3
Oleh itu: -
b)
dari Avogadro, 1 mol = 6,023 x 1023 atom, dan bahan-bahan massa atom 12g mol-1 kerana ada 2 atom dalam BCC,
itu. Mass 2 atom: - jisim 2 atom = gram = kg
Sejak, Ketumpatan = kg m3
Struktur bukan kristal
Satu bahan-bahan yang tidak mempunyai struktur unit konsisten.
Kebanyakan bahan-bahan bukan kristal adalah logam bukan. Secara umumnya bahan-bahan yang tidak mempunyai struktur kristal akan mempunyai kekuatan berbanding dengan struktur kristal.
Salah satu contoh yang kita boleh lihat sebagai struktur bukan kristal adalah bahan-bahan jenis polimer.
Bahan polimer: -
Umumnya dikenali sebagai plastik. Plastik sintetik yang dihasilkan oleh tindak balas hidrokarbon.
Plastik tidak mempunyai struktur tertentu mengulangi seperti dalam logam, tetapi terdiri daripada siri rantaian molekul, yang setiap rantaian dibentuk oleh molekul unit yang dipanggil monomer.
Sebagai contoh, keretakan ikatan karbon dua etana akan menghasilkan monomer etilena
Rajah 14: molekul etena mengandungi karbon ikatan kembar yang stabil.
Rajah 15: monomer Polyethylene sebagai unit rantaian molekul dalam polietilena polimer, n mewakili bilangan molekul yang akan membentuk rantaian molekul.
Daripada jumlah 14, kita akan lihat bahawa, karbon ikatan kembar adalah rehat ke dalam bon percuma di angka 15, ini dipanggil monomer unit yang kemudiannya membentuk satu ikatan dengan monomer lain untuk rantaian yang terbentuk daripada molekul.
Jumlah n ialah bilangan monomer yang akan membentuk rantai, yang juga akan menentukan darjah pempolimeran
Rajah 16: monomer etilena membentuk rantaian molekul
Panjang rantai polimer akan menentukan hartanya. Rantai yang lebih panjang akan membuat bahan-bahan yang lebih keras dan sukar tetapi kadang-kadang rapuh. Tinggi polimer bahan polimer ijazah sekali dikeluarkan tidak boleh cair kembali dan dikitar semula.
Panjang pendek akan menjadikan bahan yang lembut, fleksibel dan boleh cair dalam proses kitar semula.
Rajah 17: - Struktur Rangkaian dalam polietilena diletakkan secara rawak.
Mempulkanisir Getah
Getah dalam bentuk cecair (ditoreh dari pokok getah) terdiri daripada rantaian molekul tak tepu (mengandungi karbon ikatan kembar). (Rujuk rajah 18)
Semasa proses pemvulkanan, bahan tambahan seperti sulphure akan memecahkan ikatan kembar dan membentuk mempersambungkan dengan rangkaian lain.
Jika tindak balas adalah cukup besar, satu rangkaian besar rangkaian saling dibentuk itu berubah getah daripada fasa cecair kepada getah yang kukuh.
Rajah 18: Bahagian struktur rantaian yang mengandungi pautan karbon tepu (bon double).
Tambahan yang kuat seperti sulphure dapat memecahkan bon dan menghubungkan dirinya dengan rantai lain yang mengandungi karbon tepu.

Rajah 19: Ilustrasi rantaian getah mempulkanisir (struktur hubungan merentas
Bahan-bahan semula jadi: - kayu
Kayu adalah salah satu bahan yang paling banyak digunakan di dunia, dari zaman primitif kepada kayu era moden masih salah satu daripada bahan-bahan terbaik digunakan.
Kayu dibentuk oleh pembinaan dinding sel selulosa yang kuat. Yang lebih tua pokok, dinding selulosa menjadi lebih kuat dan sukar.
Rajah 18: Keratan rentas kayu. Cincin dibentuk menunjukkan usia pokok. Cincin dibentuk disebabkan oleh perubahan iklim.
Rajah 19: cincin Tahunan kayu menunjukkan pokok yang berumur 24 tahun. Teras dalam adalah lebih sukar daripada teras luar.
Rajah 20: pembentukan dinding selulosa dalam struktur kayu.
Bahan logam
Kami akan memberi tumpuan lebih kepada bahan-bahan logam jenis dalam mata pelajaran ini.
Mana-mana elemen, sebatian atau aloi yang mempunyai kekonduksian elektrik yang tinggi dipanggil logam.
Dalam logam, atom sudah bersedia untuk kehilangan elektron untuk membentuk ion + ve ion di mana mereka dikelilingi oleh delocalize elektron yang bertanggungjawab untuk kekonduksian elektrik yang tinggi.
Ikatan dalam logam dipanggil ikatan logam di mana nukleus atom adalah mengikat oleh awan elektron untuk menghasilkan ikatan.
Sifat-sifat kimia

Logam biasanya cenderung untuk membentuk kation (+ ve) melalui kehilangan elektron, bertindak balas dengan oksigen dalam udara untuk membentuk oksida lebih berubah skala masa (karat besi selama beberapa tahun, manakala kalium terbakar dalam saat).
Contoh:
4Na + O2 → 2Na2O (natrium oksida) 2Ca + O2 → 2CaO (kalsium oksida) 4Al + 3O2 → 2Al2O3 (aluminium oksida)
Logam peralihan (seperti besi, tembaga, zink, nikel) mengambil masa yang lama untuk mengoksidakan. Lain-lain, seperti palladium, platinum dan emas, tidak bertindak balas dengan suasana yang sama sekali.
Sesetengah logam membentuk lapisan halangan oksida pada permukaannya yang tidak dapat ditembusi oleh molekul oksigen lagi dan dengan itu mengekalkan penampilan berkilat dan kekonduksian yang baik untuk beberapa dekad (seperti aluminium, sesetengah keluli, dan titanium). Oksida logam secara amnya asas, berbanding dengan orang-orang bukan logam, yang berasid.
Lukisan, anodizing atau penyaduran logam adalah cara yang baik untuk mencegah kakisan mereka. Walau bagaimanapun, logam yang lebih reaktif dalam siri elektrokimia mesti dipilih untuk lapisan, terutama apabila kerepek lapisan yang dijangka. Air dan dua logam membentuk sel elektrokimia, dan jika lapisan adalah kurang reaktif daripada JAS pendek itu, salutan itu sebenarnya menggalakkan hakisan.
Ciri-ciri fizikal

Rajah 21: - kristal Gallium
Logam secara amnya mempunyai tinggi elektrik, kekonduksian terma, kilauan dan ketumpatan, dan keupayaan untuk cacat di bawah tekanan tanpa Bahawa Tuhanmu telah memerintahnya. Walaupun terdapat beberapa logam yang mempunyai ketumpatan yang rendah, kekerasan, dan takat lebur, ini (alkali dan alkali logam bumi) adalah sangat reaktif, dan jarang dijumpai dalam bentuk unsur logam mereka.
Ketumpatan
Majoriti logam mempunyai ketumpatan yang lebih tinggi daripada majoriti bukan logam. Walau bagaimanapun, terdapat perbezaan yang luas dalam ketumpatan logam; litium adalah elemen-kurangnya pepejal padat dan Osmium adalah terpadat.
Logam kumpulan IA dan II A dalam jadual berkala dirujuk sebagai logam yang ringan kerana mereka adalah pengecualian kepada umum ini.
Kemuluran
Sifat nondirectional ikatan logam dianggap sebagai sebab utama untuk kemuluran logam. Pesawat atom dalam logam yang boleh menggelongsor antara satu sama lain di bawah tekanan, iaitu keupayaan kristal untuk ubah bentuk tanpa memecahkan.
Apabila pesawat sebuah ikatan ionik akan merosot lalu satu sama lain, perubahan yang terhasil di lokasi perubahan ion caj yang sama ke dalam berdekatan, menyebabkan perpecahan kristal. Perubahan tersebut tidak diperhatikan dalam kristal covalently terikat mana patah dan dengan itu pemecahan kristal berlaku.
Bagaimana logam cacat?
Rajah 22: Ubah bentuk mekanisme untuk logam
- Panah menunjukkan daya yang bertindak ke atas struktur kristal logam
a) jika kuasa adalah cukup besar untuk cacat struktur, kolum pertama kristal akan snap daripada bon menolak ruang lain dan mengganggu struktur
b) sebagai kolum pertama menolak ruang kedua, tali leher atom dalam ruang kedua direbut tetapi membentuk kembali seri dengan ruang 1. Kesan ini akan meninggalkan kekosongan di ruangan kedua.
c) asprocesscontinueon, dislocationwillreachtheendofthecolumn mengakibatkan kecacatan kekal struktur kristal logam.
Kemuluran pelbagai jenis logam amat berbeza, dan aloi juga boleh mempunyai kemuluran yang sangat berbeza daripada logam asas. Secara umumnya, logam cenderung untuk menjadi kurang mulur pada suhu yang lebih rendah, dan juga sebagai hasil daripada kekotoran dalam logam.
Kekonduksian
Kekonduksian elektrik dan haba logam berasal dari hakikat bahawa dalam ikatan logam, elektron luar atom logam membentuk gas elektron bebas, bergerak sebagai gas elektron dalam latar belakang cas positif yang dibentuk oleh teras ion.
Aloi
Aloi adalah campuran dua atau lebih unsur-unsur dalam larutan pepejal di mana komponen utama adalah logam.
Logam yang paling tulen adalah sama ada terlalu lembut, rapuh atau kimia reaktif untuk kegunaan praktikal. Menggabungkan nisbah logam yang berlainan seperti aloi mengubah sifat logam tulen untuk menghasilkan ciri-ciri yang diingini.
Tujuan membuat aloi umumnya untuk membuat mereka kurang rapuh, keras, tahan kakisan, atau mempunyai warna yang lebih wajar dan berselerak.
Contoh aloi adalah keluli (besi dan karbon), loyang (tembaga dan zink), gangsa (tembaga dan timah), dan duralumin (aluminium dan tembaga). Aloi yang direka khas untuk aplikasi yang sangat mendesak, seperti enjin jet, mungkin mengandungi lebih daripada sepuluh unsur.
Kategori logam
Logam asas
Dalam bidang kimia, 'logam asas' istilah yang digunakan secara tidak rasmi untuk merujuk kepada logam yang mengoksidakan atau merosakkan tubuhnya yang agak mudah, dan bertindak balas variably dengan asid hidroklorik (HCl) untuk membentuk hidrogen. Contohnya termasuk besi, nikel, plumbum dan zink.
Tembaga adalah dianggap sebagai logam asas kerana ia mengoksidakan agak mudah, walaupun ia tidak bertindak balas dengan HCl. Ia biasanya digunakan dalam pembangkang kepada logam mulia.
Dalam alkimia, logam asas adalah logam biasa dan murah, berbanding dengan logam berharga, terutamanya emas dan perak.
Logam ferus
Istilah "besi" berasal dari perkataan Latin yang bermaksud "besi yang mengandungi". Ini boleh termasuk besi tulen, seperti besi tempa, atau aloi seperti keluli. Logam ferus sering magnet, tetapi tidak secara eksklusif.
Logam ferus khas dikumpulkan sejak logam ini adalah salah satu bahan yang paling penting di dunia dan digunakan secara meluas.
Logam Ferus juga mempunyai keupayaan khas yang akan dirawat dengan menggunakan rawatan haba untuk mengubah sifat-sifatnya.
Details akan dibincangkan dalam topik lain.
Logam mulia
Logam mulia adalah logam yang tahan karat atau pengoksidaan, tidak seperti logam asas yang paling. Mereka cenderung untuk menjadi logam berharga, sering kerana jarang dilihat.
Contohnya termasuk tantalum, emas, platinum, perak dan rhodium.
Logam berharga
A logam berharga adalah unsur kimia logam jarang nilai ekonomi yang tinggi.
Kimia, logam berharga adalah kurang reaktif daripada unsur-unsur yang paling, mempunyai kilauan yang tinggi dan kekonduksian elektrik yang tinggi.
Dari segi sejarah, logam berharga adalah penting sebagai mata wang, tetapi kini dianggap terutamanya sebagai pelaburan dan komoditi perindustrian.
Emas, perak, platinum dan palladium masing-masing mempunyai ISO 4217 kod mata wang. Yang paling terkenal logam berharga adalah emas dan perak.
Walaupun kedua-duanya mempunyai kegunaan industri, mereka lebih dikenali untuk kegunaan mereka dalam seni, barang kemas, dan sistem mata wang. Logam berharga lain termasuk logam kumpulan platinum: ruthenium, Rhodium, palladium, Osmium, Iridium, dan platinum, yang platinum adalah yang paling banyak diniagakan. Plutonium dan uranium juga boleh dianggap sebagai logam berharga.
Permintaan bagi logam berharga bukan sahaja didorong oleh penggunaan praktikal mereka, tetapi juga dengan peranan mereka sebagai pelaburan dan simpanan nilai. Palladium adalah, pada musim panas 2006, bernilai sedikit di bawah separuh harga emas dan platinum pada kira-kira dua kali ganda daripada emas. Perak adalah ketara kurang mahal daripada logam, tetapi sering tradisinya dianggap sebagai logam berharga untuk peranannya dalam sistem mata wang dan barang kemas.
































No comments:
Post a Comment